私たちのグループでは、
●ウイルス肝炎の免疫病態の解明と治療への応用
●肝がんの微小環境の解明と病態関連マーカー、治療法の開発
を主なテーマとして、研究室での成果を臨床に還元・応用することを目標としています
。
ウイルス性肝炎の免疫病態の解明
C型肝炎ウイルス(HCV)の感染者は日本で200万人、全世界では1億7000万人と推定されています。一方、B型肝炎ウイルス(HBV)の持続感染者は日本で130万人、全世界では3億5000万人と推定されています。日本の肝癌の約7割はHCV、約2割はB型肝炎を基盤に発症しており、肝癌の撲滅のためにはHCV、HBV感染への対策が重要となっています。
HCV感染では初感染の時に肝炎を発症する率が低いため、何の症状もなく知らぬ間に慢性肝炎や肝硬変になっている人がHCV感染者の約8割を占めています。HBVは出生時、乳幼児期に感染すると高率に持続感染が成立しキャリアとなりますが、成人に感染すると大半は急性肝炎を発症します。B型急性肝炎の発症後、約8割は免疫系の反応によって自然排除されますが、残りの2割は持続感染して慢性肝炎となります。HCVとHBVとで、感染した時の排除率や持続感染率が異なることは、ウイルスゲノム、ウイルス変異、感染者の遺伝子要因、免疫反応などの違いが関係していると推測されていますが、その全容はまだ明らかではありません。
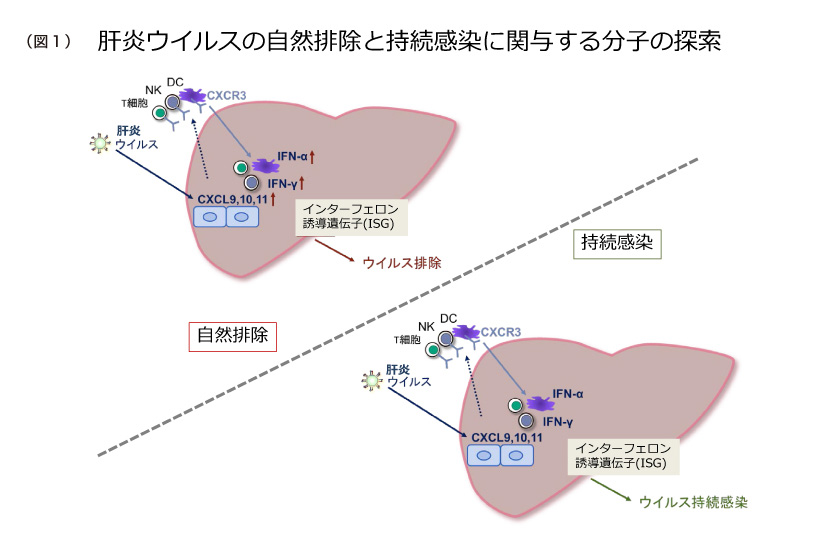
肝炎ウイルスが肝臓に感染すると、様々な免疫細胞が活性化します。特にNK細胞、マクロファージ、樹状細胞(Dendritic cell, DC)などは肝臓に多く存在しており、肝炎ウイルスの感染を察知して反応すると考えられています。その後、T細胞やB細胞などの免疫細胞が肝臓に集まり、一連の免疫反応の結果として肝炎ウイルスが排除されると考えられます。この時に免疫反応が不十分だと、肝炎ウイルスは排除されず持続感染が成立すると考えられます1-3。免疫反応の活性化には細胞間でサイトカインやケモカインという因子が関与しており、肝炎ウイルス排除の最終段階にはインターフェロンで誘導される抗ウイルス因子(Interferon-stimulated gene, ISG)が関与すると考えられます(図1)。
私たちは、患者さんの血清極少量を用いたMultiplex法を用いて、多数の免疫因子を同時に、あるいは経時的に解析し、肝炎ウイルスに対する免疫反応の全貌を捉えようとしています。患者さんの体内で起こる免疫現象を、検体から分離した免疫細胞を用いて培養プレート上で再現することで、免疫細胞による肝炎ウイルス感染細胞の認識機序や細胞間の相互作用を明らかにし、難治性ウイルス性肝炎の治療法の開発に繋げることを目標にしています。
1. Kanto, T. Dendritic cells in hepatitis virus infection: a legatus within. Current Immunology Reviews 2011
2. Kanto, T., Virus associated innate immunity in liver. Front Biosci 2008. 13: 6183-6192.
3. Yoshio, S., Kanto, T. et al. Human BDCA3+ dendritic cells are a potent producer of IFN-![]() in response to
in response to
hepatitis C virus. Hepatology 2013 57: 1705-1715.
肝がんの微小環境の形成機序の解明から治療法の開発へ
近年、C型慢性肝炎に対する治療は劇的に進歩し、従来のインターフェロンを基本とする治療よりも、短期間でかつ高いウイルス排除率が得られるようになって来ました。2015年3月現在、インターフェロンを用いない経口薬のみの治療も可能となっていますが、今後も新薬が臨床現場に登場する予定です。C型慢性肝炎の治療成績が向上し、さらにHCV関連肝癌は減少することが期待されています。B型慢性肝炎に対しても、核酸アナログ製剤とインターフェロンによる治療が標準化し、長期的なHBV複製の抑制によって、発がん率が低下することが示されています。以上のように、ウイルス性肝癌の発症予防の戦略はある程度確立してきたといえます。
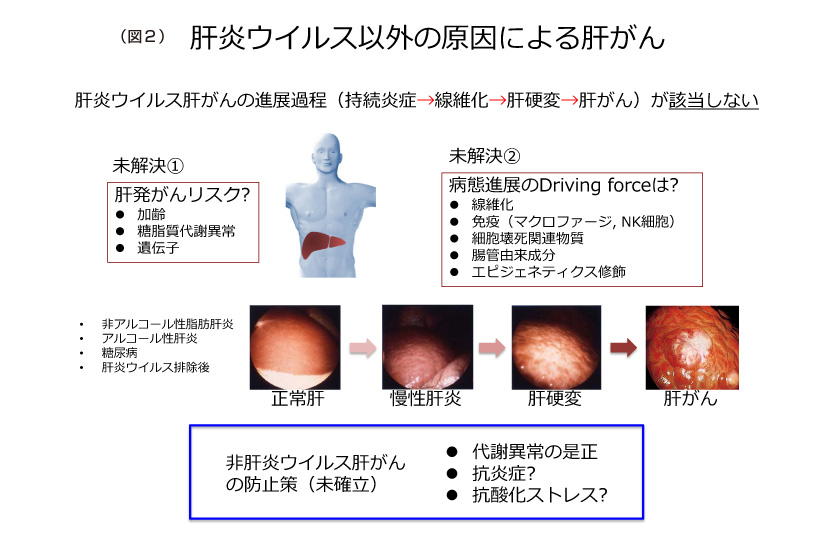
一方で、肝炎ウイルス性以外の慢性肝炎(アルコール性肝炎、非アルコール性脂肪肝炎など)や糖尿病を基盤とする非ウイルス性肝がんは、日本でも着実に増えています。これらは発がんの危険因子は明らかではありませんし、肝炎から肝硬変、肝がんへと肝臓病を促進させる因子も明らかではありません。非ウイルス性肝がんの対策は、未だ確立されていないのが現状です(図2)。
肝がんに限らず、がん細胞は増殖する時に周囲の環境(がん微小環境と言います)からのサポートが必要です。がんの微小環境を構成するのは、線維芽細胞、マクロファージや樹状細胞などの免疫細胞、腫瘍血管新生細胞1などです。近年の研究によって、がんの増殖や転移には、がん細胞と微小環境構成細胞との相互作用が重要であり、その細胞間の連携を断ち切ることで、がんの悪性化や転移が抑えられることが分かってきました。
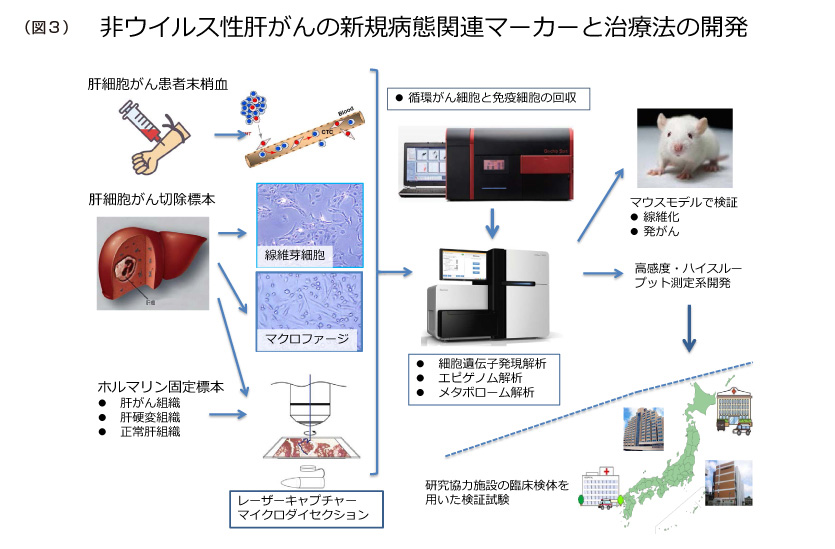
私たちは、患者さんの検査や治療によって得られた検体からがん細胞、線維芽細胞、免疫細胞などを採取して、細胞の機能や遺伝子を調べることで、肝癌の微小環境の成り立ちを解き明かし、発がんのリスク因子やがん細胞の性質に関わる重要な分子を明らかにしたいと考えています。がん細胞と微小環境細胞との連携に関わる分子は、新たな診断マーカーや治療の標的になる可能性を持っています。将来的には、多数の臨床検体でその有用性を検証したいと考えています(図3)。
1. Matsubara, T., Kanto, T. et al. TIE2-expressing monocytes as a diagnostic marker for hepatocellular
carcinoma correlated with angiogenesis. Hepatology 2013 57: 1416-1425